Aluminium ist nach Sauerstoff und Silicium das dritthäufigste Element in der Erdkruste. Es kommt zwar sehr häufig vor, aber niemals in seiner reinen Form. Daher kann der Werkstoff nicht einfach in der Natur abgebaut werden, sondern wird in einem aufwändigen Verfahren hergestellt. Was für ein Rohstoff steckt hinter Aluminium? Welche Prozesse müssen durchlaufen werden, um am Ende reines Aluminium zu erhalten?
Die Grundlage: Bauxit
Aluminium findet man in der Natur nur in Aluminiumverbindungen. Die höchste Aluminium-Konzentration befindet sich in sogenannten Bauxiten - das sind Verwitterungsprodukte aus Kalk- und Silikatgestein. In Bauxit beträgt der Anteil von Aluminiumoxiden häufig über 50 Prozent. Das ist der Rohstoff für die Aluminiumproduktion. Die größten Abbaugebiete befinden sich in Australien, China, Guinea, Brasilien und Indien. An solchen Orten enthält der Rohstoff die größte Menge an Alumerde - reines Aluminiumoxid. Alumerde wird meist an dem Abbauort des Bauxits gewonnen. Das spart Transportkosten. Wie funktioniert das?
Die Umwandlung: Alumerde
Durch das Bayer-Verfahren, erfunden 1887 und benannt nach Karl Bayer, wird aus dem Bauxit das reine Aluminiumoxid - Alumerde oder auch Tonerde genannt - gewonnen. Bauxit wird in großen Mengen fein gemahlen. Danach wird es in einen großen Behälter gefüllt und mit erhitzter Natronlauge ergänzt; eine Lösung aus ätzendem Soda und Wasser, die das Aluminiumoxid im Bauxit löst. Aluminiumslurry nennt man das flüssige Gemisch aus Natronlauge und dem darin gelösten Aluminiumoxid. Rotschlamm sind die nicht gelösten Bauxit-Bestandteile.
Mithilfe von Filtern wird die Aluminiumslurry vom Rotschlamm getrennt. Letzteres wird entsorgt. Die Aluminiumslurry wird gekühlt und in Silos gepumpt. Es entstehen kleine, weiße Kristalle in der Flüssigkeit, die zu Boden sinken. Sie werden in einen weiteren Silo umgeleitet, in dem die Kristalle weiter wachsen können. Bei einer Temperatur von 1000°C werden die Kristalle in einem Ofen zu Alumerde, reines Aluminiumoxid, umgewandelt: ein feines, weißes Pulver entsteht. Wie wird nun daraus Aluminium produziert?
Die Gewinnung: der Elektrolyseprozess
Für die Alumerde geht es weiter in die primären Schmelzöfen. Die sogenannten Aluminiumhütten befinden sich oft an Standorten, an denen preiswerte und relativ sauberer Energie erzeugt werden kann. Durch das Hall-Héroult-Verfahren wird aus Alumerde reines Aluminium erzeugt. Ein Verfahren, benannt nach zwei Forschern, die diese Methode unabhängig voneinander im Jahr 1886 erfunden haben.
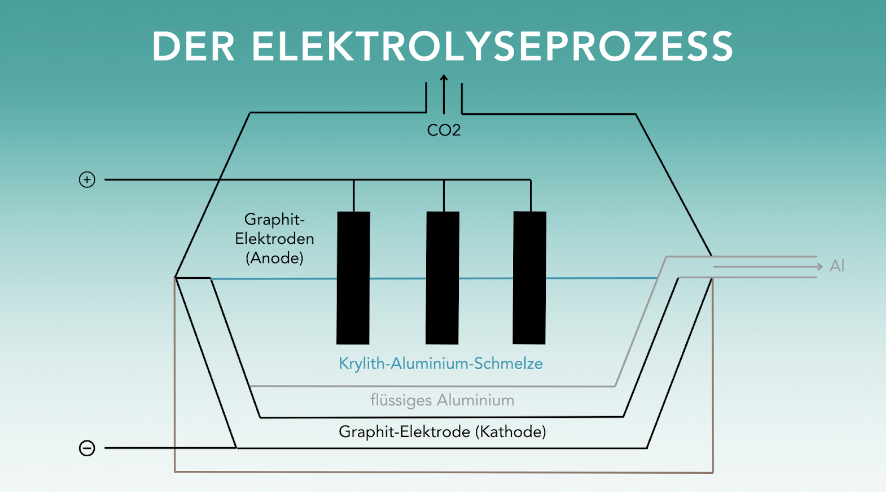
Alumerde besteht aus Aluminium und Sauerstoff. Das Hall-Héroult-Verfahren trennt im Rahmen der Schmelzflusselektrolyse beides voneinander. Die Alumerde kommt in ein Reduziergefäß. In diesem Gefäß befindet sich das Fluoridsalz Kryolith, erhitzt auf 1000°C. Die Innenseite des Gefäßes ist oft mit Graphit bedeckt. Zwischen den drei Anodenblöcken aus Kohlenstoff, die in dem Gefäß hängen, und dem Graphit wird eine elektrische Spannung erzeugt. Diese ist zwar niedrig (4 bis 5 Volt), hat aber eine extrem hohe Stromstärke von 220.000 bis 340.000 Ampère. Der elektrische Strom trennt den Sauerstoff vom Aluminium. Der Sauerstoff bindet sich an den Kohlenstoff der Anodenblöcke und wird in Form von CO² entsorgt. Das reine Aluminium sinkt zu Boden und wird in flüssigem Zustand abgelassen. Das flüssige Aluminium wird in Formen gegossen. Nun kann es für verschiedenen Zwecke weiterverarbeitet werden.